Заболевания глазной поверхности: влияние на предоперационные данные биометрии и на симптомы после рефракционных операций и хирургии катаракты.
Ключевые тезисы
- Дефекты слезной пленки на фоне синдрома сухого глаза (ССГ) могут значительно влиять на предоперационные биометрические измерения, необходимые для точного расчёта плана операции.
- Синдром сухого глаза широко распространён среди пациентов, которым планируется хирургическое вмешательство. Без лечения субъективные дискомфортные ощущения у них сохраняются и усугубляются, а неточные биометрические данные могут приводить к ошибкам расчёта интраокулярной линзы (ИОЛ), необходимой для хирургии.
- Разработаны специальные алгоритмы, чтобы помочь врачам тщательно и эффективно диагностировать и лечить ССГ, с целью улучшения качества слёзной плёнки и уменьшения симптомов, важных для успеха хирургии.
Введение
Качество слезной пленки важно для сохранения здоровья глазной поверхности и обеспечения хорошего зрения и комфорта пациента. Патологические изменения слезной плёнки на фоне ССГ могут приводить к повышению испарения водного компонента, воспалению глазной поверхности и симптомам дискомфорта, а также расплывчатому или нестабильному зрению. ССГ очень часто встречается после рефракционных операций и хирургии катаракты. 91% хирургов полагают, что ССГ легкой и средней степени влияет на удовлетворенность пациентов после операции1. Исторически сложилось так, что диагностику ССГ, как правило, проводят только пациентам при наличии симптомов, при этом приблизительно половина тех, кому планируется хирургия катаракты, имеют клинические признаки патологии глазной поверхности при отсутствии субъективных симптомов, и ССГ у них не диагностируется до операции2, 3. Предоперационное лечение помогает улучшить качество слёзной плёнки, что приводит к более точным биометрическим измерениям и уменьшает симптомы ССГ4. Таким образом, происходит смена парадигмы предоперационного ведения: приоритетом становится диагностика и лечение ССГ до операции с целью оптимизации биометрических показателей и улучшения субъективных ощущений пациента1.
Распространённость заболеваний глазной поверхности среди пациентов с показаниями к рефракционной и катарактальной хирургии
В мировой практике факоэмульсификация (ФЭК) является самой распространенной хирургической процедурой в офтальмологии, а рефракционные операции относятся к самым популярным плановым вмешательствам в США. В 2017 году около 700000 американцев прошли через рефракционную хирургию, и приблизительно 3,8 млн прооперированы по поводу катаракты, согласно данным Market Scope5, 6. Примерно 9,8% и 6,0% пациентов отмечают симптомы ССГ после катарактальной и рефракционной хирургии, соответственно7, 8. После LASIK его распространенность может составлять от 20 до 53%9, 10. Хотя выделяют несколько факторов риска послеоперационного развития ССГ, одним из наиболее важных из них является наличие недиагностированной и нелеченной до проведения вмешательства патологии глазной поверхности. В нескольких работах изучалась распространённость ССГ, выявленного на предоперационном обследовании, у пациентов с показаниями к рефракционной и катарактальной хирургии. Поскольку практические специалисты используют большое разнообразие диагностических инструментов для определения наличия и степени выраженности ССГ, данные по его распространённости варьируются, в зависимости от того, какие диагностические тесты применялись в исследовании11.
Что касается рефракционной хирургии, симптомы ССГ до операции были выявлены у 38% пациентов, которым был далее сделан LASIK, и у 48% пациентов, которым планировалось проведение фоторефракционной кератэктомии12, 13. Альбейтц (Albeitz) и соавторы провели осмотр 565 пациентов перед LASIK и обнаружили ССГ у 7% из них, в то время как еще 18% отмечали наличие симптомов ССГ, но не имели объективных клинических признаков заболевания14.
Гупта (Gupta) и соавторы обследовали 120 пациентов, обратившихся по поводу катаракты, с помощью ряда диагностических тестов на ССГ, включавших проверку осмолярности слезной плёнки, содержания
Авторы других работ основывались на более традиционных диагностических тестах и обнаружили еще более высокую распространенность патологии глазной поверхности. Треттлер (Trattler) и соавторы обследовали перед операцией 136 пациентов с катарактой: у 69,2% выявлено время разрыва слезной пленки (ВРСП) с флюоресцеином <5 секунд, окрашивание роговицы отмечено у 77% глаз (50% глаз — центральное окрашивание роговицы), результат теста Ширмера с анестезией <5mm имели 18% пациентов15. Кошенер (Cochener) и другие обследовали 180 пациентов с катарактой (342 глаза) на наличие признаков дисфункции мейбомиевых желез (ДМЖ) и обнаружили, что 54% пациентов имели низкую экспрессию мейбомиевых желез и 56% пациентов имели атрофию мейбомиевых желез в той или иной степени2. Среди пациентов без симптомов 71% имели низкую экспрессию МЖ и/или их атрофию. Наконец, Визо (Viso) и соавторы обследовали 619 пациентов на наличие признаков ДМЖ, таких как наличие вязкого или воскообразного белого секрета при компрессионной пробе, двух или более телеангиэктазий по краю век и двух или более закупоренных устьев желез16. По результатам исследования, в среднем у 21,9% пациентов выявлена бессимптомная ДМЖ и у 8,6% — ДМЖ с наличием симптомов.
Таким образом, распространенность ССГ может широко варьироваться, в зависимости от использующихся диагностических тестов и критериев. Однако результаты исследований свидетельствуют, что значительное количество бессимптомных пациентов (50–71%) могут иметь множественные клинические признаки патологии глазной поверхности. Так как эти пациенты не предъявляют жалобы и не сообщают о симптомах на этапе предоперационного обследования, патологические изменения у них зачастую не диагностируются, а следовательно, остаются без лечения.
Слёзная плёнка и биометрические показатели
Для того, чтобы понимать возможные последствия проведения рефракционной операции или ФЭК пациенту с некомпенсированным ССГ, необходимо оценить какой эффект оказывает состояние слезной пленки на предоперационные измерения, включающие в себя кератометрию, кератотопографию и анализ волнового фронта. В основе этих методов исследования лежит измерение либо проекций света, проходящего через слезную пленку, либо лучей света, отраженных от слёзной плёнки. Вследствие изменения коэффициента преломления на границе раздела сред
Граница раздела сред

Эпитропулос (Epitropoulos) и соавторы обнаружили, что у пациентов с гиперосмолярной слезной жидкостью (> 316 мОсм/л хотя бы в одном глазу) значительно больше варьировались данные средней кератометрии и переднего роговичного астигматизма, чем у пациентов с нормальной осмолярностью слезы (<308 мОсм / л в обоих глазах) (p = 0,05), и это приводило к выраженным различиям в расчетах оптической силы ИОЛ (p = 0,02)21. Авторы предполагают, что оценка осмолярности слезной жидкости на этапе предоперационного обследования может эффективно выявлять пациентов с риском неожиданно высокой рефракционной ошибки вследствие неточной кератометрии.
Матосян (Matossian) опубликовала результаты пилотного исследования, посвященного изучению вопроса, может ли лечение методом тепловой пульсации век повлиять на предоперационные кератометрические измерения. Она обнаружила, что у всех 24 пациентов, принимавших участие в работе, наблюдались значимые изменения
Помимо влияния на объективные данные биометрии, нестабильная слезная пленка также может приводить к колебаниям качества зрения. Группа исследователей в области диагностики и лечения ССГ, The Dry Eye Assessment and Management (DREAM), обнаружили связь между наличием клинических признаков и субъективных симптомов ССГ и показателями контрастной чувствительности и остроты зрения. Среди 487 участников исследования худший средний балл по индексу заболеваний глазной поверхности (OSDI) коррелировал с наибольшим снижением остроты зрения (p = 0,02)23. Выраженная закупорка мейбомиевых желез и патологические изменения секреции, а также более короткое ВРСП были связаны с ухудшением контрастной чувствительности (p = 0,04 и p <0,001 соответственно).
Дефекты слезной пленки, как показали эти исследования, могут на предоперационном этапе оказывать влияние на остроту зрения и контрастную чувствительность, биометрические измерения и, в конечном итоге, на расчет оптической силы ИОЛ.
Предоперационная диагностика и лечение синдрома сухого глаза
Вследствие распространённости синдрома сухого глаза у пациентов, которым планируется хирургическое лечение, и потенциального влияния некомпенсированного ССГ на результаты предоперационного обследования, наблюдается рост интереса офтальмохирургов к методам диагностики и лечения ССГ на дооперационном этапе. Однако, согласно результатам опроса хирургов, проведенного ASCRS, ССГ и другие заболевания глазной поверхности часто вызывают замешательство у специалистов. Более 75% респондентов были незнакомы с обществом исследователей слёзной плёнки и глазной поверхности, Tear Film & Ocular Surface (TFOS) Society, и рабочей группой по ССГ, Dry Eye Workshop (DEWS) II, которые публиковали обширные сведения по эпидемиологии, патофизиологии, диагностике и методам лечения ССГ1. Ниже приводится краткое изложение руководств TFOS DEWS II и ASCRS по предоперационной диагностике и лечению ССГ1, 24. ССГ — мультифакторное заболевание, которое зачастую требует комплексной диагностики и лечения. Однако систематический подход к обследованию глазной поверхности может помочь установить диагноз, определиться с тактикой ведения пациента и дать рекомендации по лечению.
Диагностика
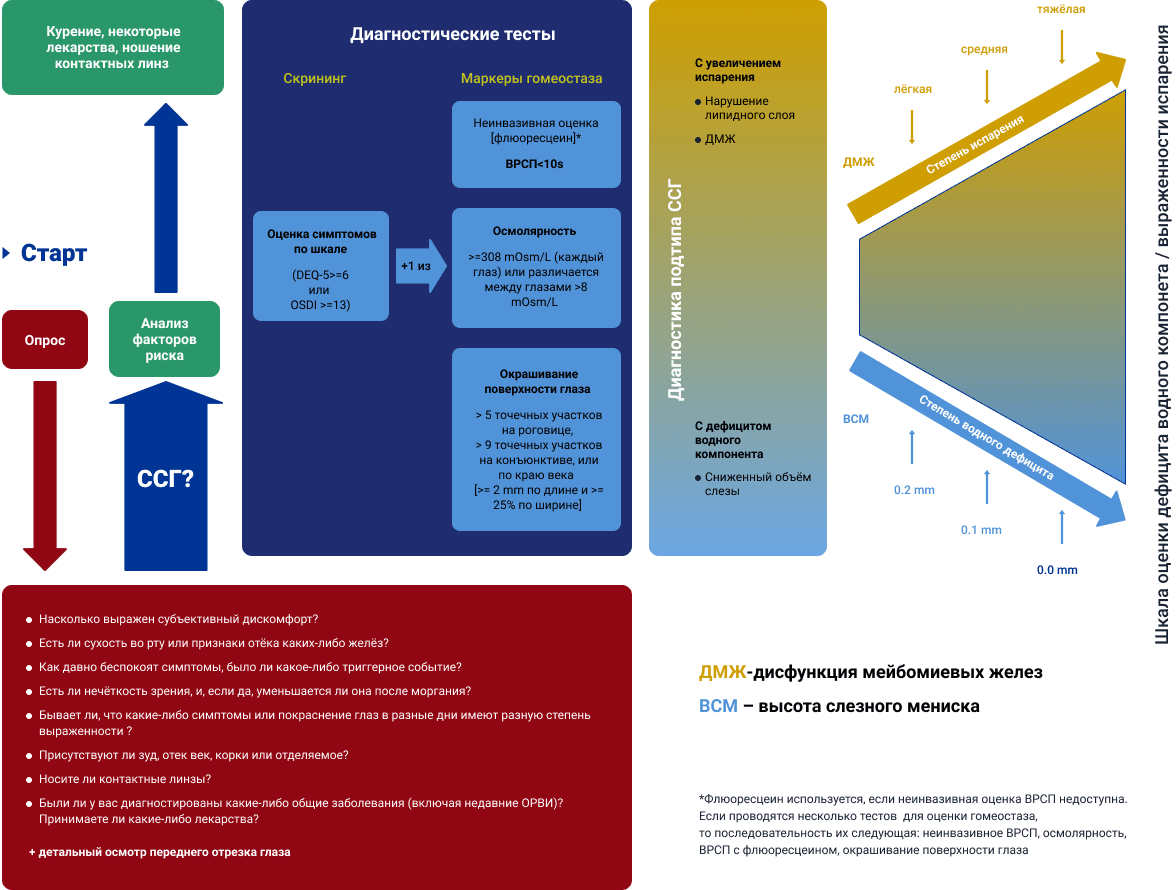
Алгоритм диагностики ССГ TFOS DEWS II (рисунок 2) направлен на определение основной причины развития дискомфортных симптомов, чтобы лечение также могло быть более целенаправленным24. Список отборочных вопросов разработан, чтобы исключить состояния, которые могут имитировать ССГ, а анализ факторов риска помогает определиться с итоговой тактикой лечения. После стандартизированных вопросов анкеты следует перейти к диагностическим тестам оценки ВРСП, осмолярности и/или окрашивания поверхности глаза флуоресцеином и лиссаминовым зеленым (осмотр роговицы, конъюнктивы и края века). Оценка признаков ДМЖ, включающая определение качества и количества секрета желез, а также объема слезы, нужна, чтобы классифицировать подтип ССГ — преимущественно с дефицитом водного компонента или увеличением испарения. Выраженная симптоматика при отсутствии объективных клинических признаков ССГ может свидетельствовать о боли невропатического характера. При наличии только клинических признаков может потребоваться лечение, чтобы предотвратить развитие ССГ и восстановить гомеостаз глазной поверхности. На рисунке 3 представлены рекомендации по диагностике и ведению пациента при наличии или отсутствии субъективных симптомов и клинических признаков ССГ.
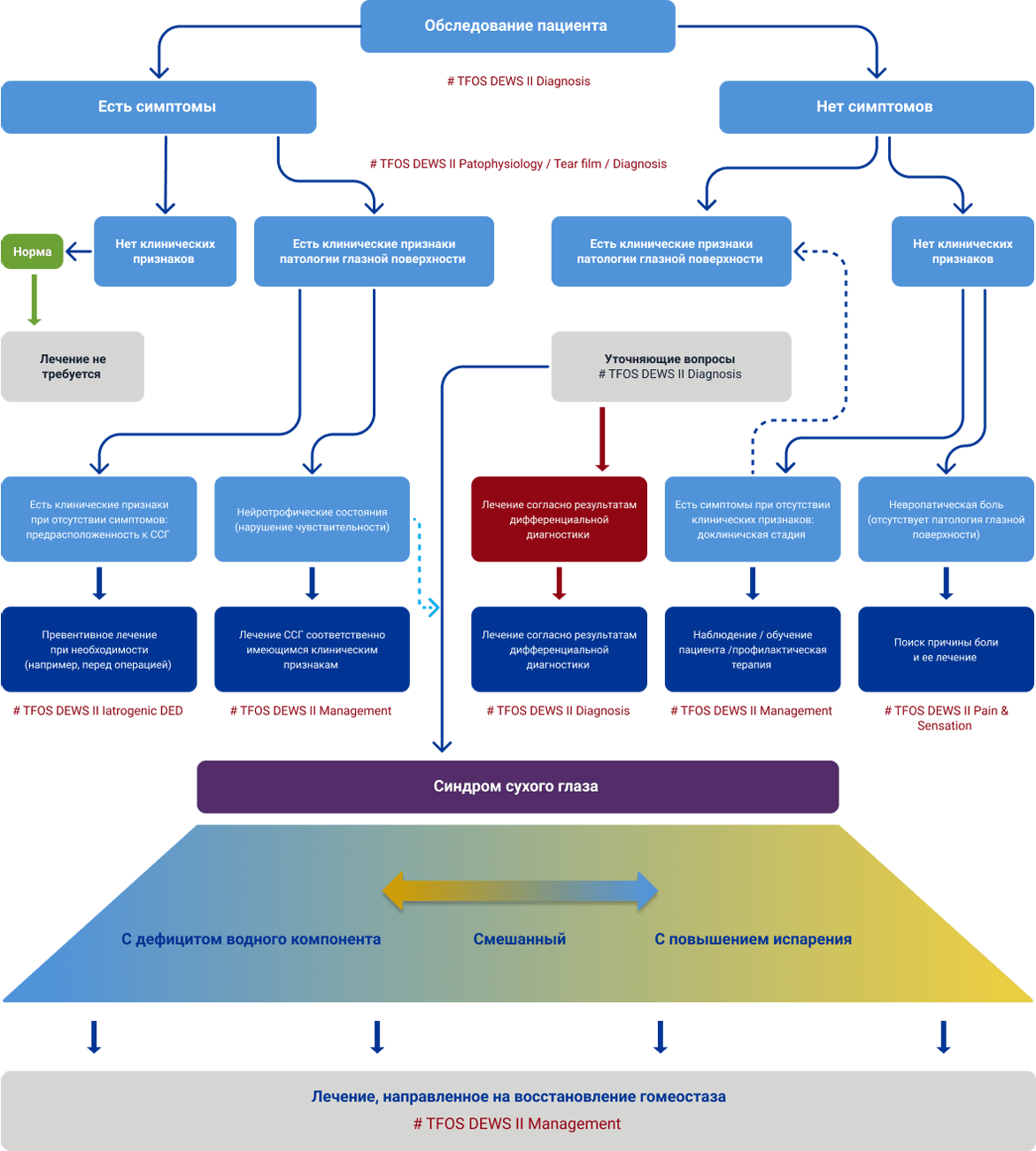
Клинический комитет ASCRS по роговице, The ASCRS Cornea Clinical Committee, разработал алгоритм предоперационного ведения пациентов с заболеваниями глазной поверхности, the Preoperative Ocular Surface Disease Algorithm (Рис. 4 и 5). В этом алгоритме акцент сделан на объективные, неинвазивные диагностические тесты, которые могут выполняться средним медицинским персоналом1. Такая тактика обоснована тем, что предоперационные осмотры уже включают в себя значительный объем рефракционных и биометрических исследований, которые часто проводит средний медицинский персонал, поэтому данный алгоритм помогает сэкономить время работы врача.
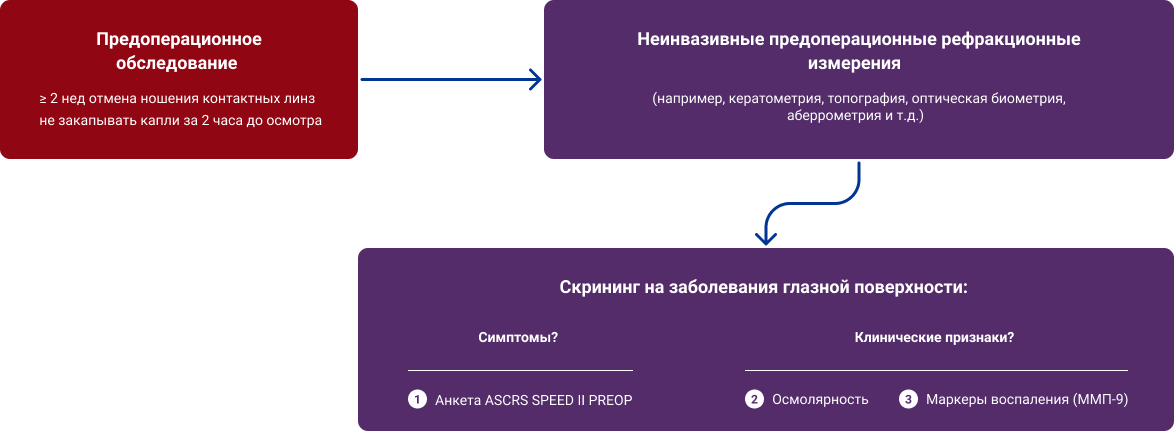
На Рисунке 4 представлены элементы первичного скрининга, который также может выполнять средний медицинский персонал, проведение этих исследований на предоперационном этапе рекомендовано Клиническим комитетом ASCRS по роговице. Диагностика включает опросник — стандартную анкету пациента для выявления сухости глаз, ASCRS Standard Patient Evaluation of Eye Dryness (SPEED) II, измерение осмолярности слёзной жидкости и тест на содержание матриксной
Согласно рекомендациям ASCRS, если по
После предварительной диагностики, вне зависимости от ее результатов, необходимо провести обследование «Посмотри, подними, потяни и нажми» («Look, Lift, Pull, and Push»), которое имеет ключевое значение (рисунок 5)1. «Посмотри» — это визуальная оценка состояния век, ресниц и глазной поверхности. «Подними и потяни» — это выворот век для оценки наличия дистрофии эпителиальной базальной мембраны и атонии век. «Нажми» предполагает пальпаторное давление на нижнее веко для оценки качества и количества секрета, экспрессируемого мейбомиевыми железами.

Заключительный этап обследования считается инвазивным и включает в себя использование распространенных витальных красителей, таких как флуоресцеин натрия (для измерения ВРСП и оценки окрашивания роговицы), и лиссаминовый зеленый или бенгальский розовый для окрашивания омертвевших клеток эпителия1.
TFOS DEWS II и ASCRS предлагают различные алгоритмы для диагностики и лечения ССГ, варьирующиеся в зависимости от клинических условий. Общий принцип — провести небольшой набор скрининговых тестов, как субъективных, так и объективных, чтобы определить, требуется ли более углубленная диагностика. Так как качество слёзной плёнки имеет критически важное значение для точности кератометрии, и эти измерения необходимы для успешного расчета параметров ФЭК и рефракционной хирургии, рекомендуется, чтобы все пациенты в процессе подготовки к хирургическому вмешательству, проходили обследование для выявления заболеваний глазной поверхности и, при наличии показаний, получали соответствующее лечение. Это необходимо, чтобы оптимизировать предоперационные биометрические измерения и улучшить послеоперационные результаты.
Лечение
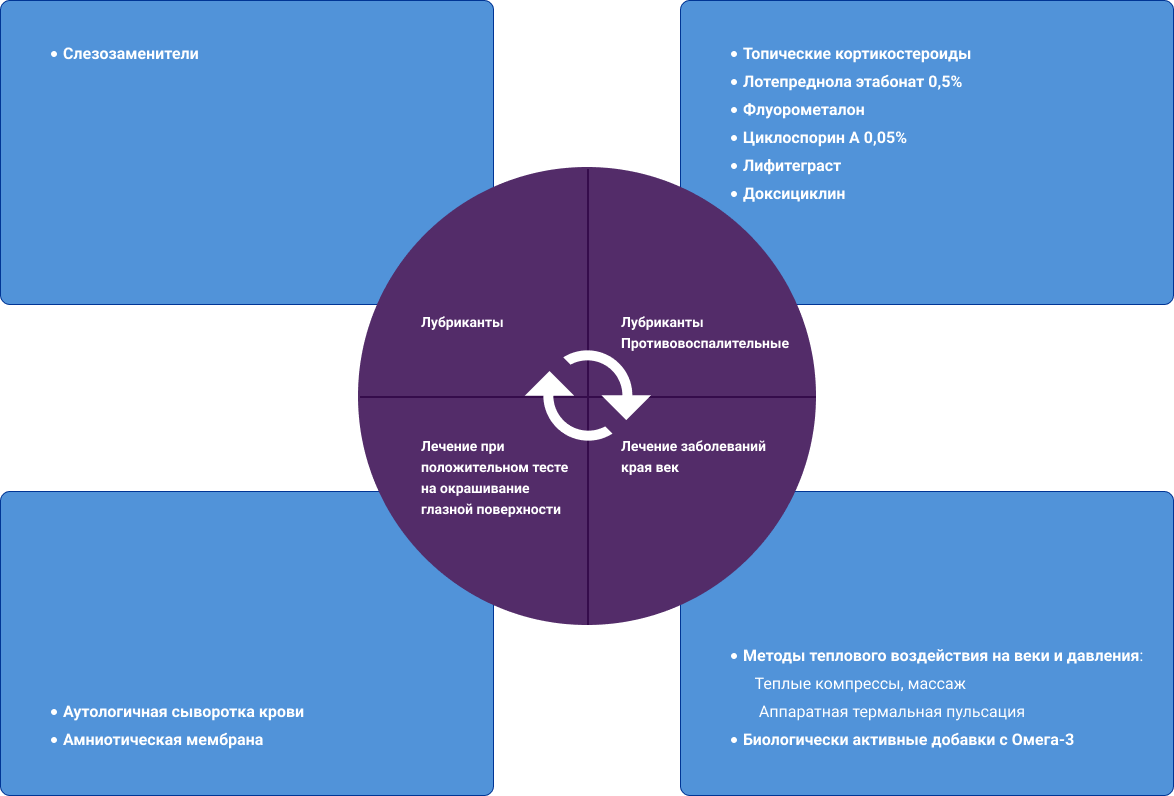
Рекомендации по лечению ранее подробно обсуждались Международной рабочей группой по дисфункции мейбомиевых желез (the International Workshop on Meibomian Gland Dysfunction), а также приведены в отчете DEWS II, но, если клинически значимая патология глазной поверхности выявляется во время предоперационного обследования, группа ASCRS рекомендует более активную тактику лечения1. Это связано с необходимостью быстро восстановить гомеостаз, чтобы обеспечить точные предоперационные измерения и максимальный послеоперационный результат. Цель состоит в том, чтобы минимизировать время ожидания операции за счёт одновременной работы с разными процессами — воспалением глазной поверхности, окрашиванием роговицы и патологией края век. Краткое изложение вариантов лечения, рекомендованных Клиническим комитетом ASCRS по роговице (the ASCRS Cornea Clinical Committee) представлено в Таблице 11.
Заключение
Приблизительно 50% пациентов, которым планируется хирургическое вмешательство, имеют субъективные симптомы и клинические признаки ССГ, и более, чем у половины пациентов, не имеющих жалоб, во время осмотра выявляются объективные признаки патологии глазной поверхности2, 7, 9, 10, 13-15. Так как результаты предоперационных биометрических измерений зависят от качества слёзной плёнки, диагностика и лечение ССГ до проведения рефракционной операции или ФЭК помогают оптимизировать данные биометрии и уменьшить симптомы, важные для успеха хирургии впоследствии. Методы диагностики и лечения ССГ всегда комплексные. Чтобы облегчить эти процессы, подробные алгоритмы разработаны и опубликованы в научной литературе (TFOS DEWS II report и the ASCRS Preoperative Ocular Surface Disease Algorithm). В исследованиях показано, что лечение ССГ повышает точность кератометрии и уменьшает выраженность симптомов, поэтому предоперационный скрининг, углублённая диагностика (по показаниям), обоснованное лечение и выбор дальнейшей тактики ведения пациента с патологией глазной поверхности очень важны.
ИНФОРМАЦИЯ ПРЕДНАЗНАЧЕНА ДЛЯ МЕДИЦИНСКИХ И ФАРМАЦЕВТИЧЕСКИХ РАБОТНИКОВ
Ссылки
- Starr CE, Gupta PK, Farid M, Beckman KA, Chan CC, Yeu E, Gomes JAP, Ayers BD, Berdahl JP, Holland EJ, Kim T, Mah FS, ASCRS Cornea Clinical Committee. An algorithm for the preoperative diagnosis and treatment of ocular surface disorders. J Cataract Refract Surg 2019;45:669–84.
- Cochener B, Cassan A, Omiel L. Prevalence of meibomian gland dysfunction at the time of cataract surgery. J Cataract Refract Surg 2018;44:144–8.
- Gupta PK, Drinkwater OJ, VanDusen KW, Brissette AR, Starr CE. Prevalence of ocular surface dysfunction in patients presenting for cataract surgery evaluation. J Cataract Refract Surg 2018;44:1090–6.
- Song P, Sun Z, Ren S, Yang K, Deng G, Zeng Q, Sun Y. Preoperative Management of MGD Alleviates the Aggravation of MGD and Dry Eye Induced by Cataract Surgery: A Prospective, Randomized Clinical Trial. Biomed Res Int 2019;2019:2737968.
- iData Research. Over 3.8 Million Cataract Surgeries Performed Every Year — iData Research. iData Res — Intell Behind Data 2018.
- LASIK: Know the Rewards and the Risks.
- Kasetsuwan N, Satitpitakul V, Changul T, Jariyakosol S. Incidence and pattern of dry eye after cataract surgery. Wedrich A, ed. PLoS One 2013;8:e78657.
Shehadeh-Mashor R, Mimouni M, Shapira Y, Sela T, Munzer G, Kaiserman I. Risk Factors for Dry Eye After Refractive Surgery. Cornea 2019;38:1495–9.- Shoja MR, Besharati MR. Dry eye after LASIK for myopia: Incidence and risk factors. Eur J Ophthalmol 2007;17:1–6.
- De Paiva CS, Chen Z, Koch DD, Hamill MB, Manuel FK, Hassan SS, Wilhelmus KR, Pflugfelder SC. The incidence and risk factors for developing dry eye after myopic LASIK. Am J Ophthalmol 2006;141:438–45.
- Stapleton F, Alves M, Bunya VY, Jalbert I, Lekhanont K, Malet F, Na
K-S , Schaumberg D, Uchino M, Vehof J, Viso E, Vitale S, Jones L. TFOS DEWS II Epidemiology Report. Ocul Surf 2017;15:334–65. - Albietz JM, Lenton LM, McLennan SM. The effect of ocular surface management on myopic lasik outcomes. Cornea 2000;19.
- Corbett MC, O’Brart DPS, Warburton FG, Marshall J. Biologic and Environmental Risk Factors for Regression after Photorefractive Keratectomy. Ophthalmology 1996;103:1381–91.
- Albietz JM, Lenton LM, McLennan SG, McLennan SG. Chronic dry eye and regression after laser in situ keratomileusis for myopia. J Cataract Refract Surg 2004;30:675–84.
- Trattler WB, Majmudar PA, Donnenfeld ED, McDonald M, Stonecipher KC, Goldberg D. The Prospective Health Assessment of Cataract Patients’ Ocular Surface (PHACO) study: the effect of dry eye. Clin Ophthalmol 2017;Volume 11:1423–30.
- Viso E, Rodrí
guez-Ares MT, Abelenda D, Oubiña B, Gude F. Prevalence of Asymptomatic and Symptomatic Meibomian Gland Dysfunction in the General Population of Spain. Investig Opthalmology Vis Sci 2012;53:2601. - Lawrenson JG. Anterior Eye. Contact Lens Pract January 2018:10–27.e2.
- Holladay JT. Accurate Corneal Power Measurements for IOL Calculations. Ocul Surg News US Ed 2016.
- Wong TA, Petito GT. The Ins and Outs of Wavefront Aberrometry. Rev Cornea Contact Lenses 2018.
- de Paiva CS, Lindsey JL, Pflugfelder SC. Assessing the severity of keratitis sicca with videokeratoscopic indices. Ophthalmology 2003;110:1102–9.
- Epitropoulos AT, Matossian C, Berdy GJ, Malhotra RP, Potvin R. Effect of tear osmolarity on repeatability of keratometry for cataract surgery planning. J Cataract Refract Surg 2015;41:1672–7.
- Matossian C. Effect of Thermal Pulsation System Treatment on Keratometry Measurements Prior to Cataract Surgery |ASCRS. In: American Society of Cataract and Refractive Surgery. Vol; 2019.
Szczotka-Flynn LB, Maguire MG, Ying G, Lin MC, Bunya VY, Dana R, Asbell PA. Impact of Dry Eye on Visual Acuity and Contrast Sensitivity. Optom Vis Sci 2019;96:387–96.- Wolffsohn JS, Arita R, Chalmers R, Djalilian A, Dogru M, Dumbleton K, Gupta PK, Karpecki P, Lazreg S, Pult H, Sullivan BD, Tomlinson A, Tong L, Villani E, Yoon KC, Jones L, Craig JP. TFOS DEWS II Diagnostic Methodology report. Ocul Surf 2017;15:539–74.
- Research in dry eye: report of the Research Subcommittee of the International Dry Eye WorkShop (2007). Ocul Surf 2007;5:179–93.
- Sambursky R, Davitt WF, Latkany R, Tauber S, Starr C, Friedberg M, Dirks MS, McDonald M. Sensitivity and Specificity of a
Point-of-Care Matrix Metalloproteinase 9 Immunoassay for Diagnosing Inflammation Related to Dry Eye. JAMA Ophthalmol 2013;131:24.
Материалы Клуба PROфессионалов предназначены только для медицинских работников. Если вы являетесь медицинским работником, то для регистрации вам необходимо перейти в личный кабинет и заполнить данные о специалисте
Материалы предназначены только для медицинских работников
Данный раздел сайта содержит информацию, предназначенную только для медицинских и фармацевтических работников.
Вы являетесь медицинским или фармацевтическим работником?
